Die Albumin-Carrier-Therapie ist eine nebenwirkungsarme Form für die Behandlung von Tumoren, Metastasen und Entzündungen. Der Wirkstoff wird dabei an das im Blut vorkommende Protein Albumin gekoppelt und so auf natürliche Weise direkt in die Tumorzellen transportiert.
In den 50er Jahren erkannten US-Wissenschaftler, dass das im Blut vorkommende Protein Albumin als Transporter in Tumoren für Medikamente genutzt werden kann. Ende der 90er Jahre gelang es Dr. Hannsjörg Sinn und seinem Team vom Deutschen Krebsforschungszentrum, Heidelberg, erstmalig, diesen Carrier medizinisch zu nutzen. Dr. Sinn konnte sein Lebenswerk nicht mehr zur Zulassung führen. Dieses Ziel verfolgen jetzt Petra und Michael Denck mit der privaten Initiative Albumin-Carrier-Therapie.
Gezielte Therapie bei Tumorerkrankungen
Ein Tumor besteht aus entarteten, unkontrolliert wachsenden Zellen, die in das umliegende gesunde Gewebe wuchern. Tumorzellen vermehren sich sehr schnell und haben daher viel mehr Bedarf an Energie und Stickstoffverbindungen als gesunde Zellen. Um diesen Bedarf zu decken, nehmen die Krebszellen besonders viel Protein, insbesondere Serumalbumin (HSA), aus dem Blut auf, während dies bei gesunden Zellen nicht der Fall ist.
MTX-HSA – der Beginn von albumingebundenen Wirkstoffen

Dr. Hannsjörg Sinn † als Senior Scientist beim Deutschen Krebsforschungszentrum (DKFZ) in Heidelberg
Dr. Hannsjörg Sinn † war als Senior Scientist beim Deutschen Krebsforschungszentrum (DKFZ) in Heidelberg im Bereich Radiochemie und Radiopharmakologie tätig. Er entdeckte einen Weg, wie bereits zugelassene Wirkstoffe, wie z.B. Methotrexat (MTX) erfolgreich an Albumin als Carrier gekoppelt werden können, um sie nach dem trojanischen Prinzip in Tumorzellen einzuschleusen. Dieser ideale Träger verbirgt den Wirkstoff so lange bis er im Zielort, dem Tumor, enzymatisch freigesetzt wird. So kann das kranke Gewebe gezielt therapiert werden.
Schonende und längere Wirkung
Durch die selektive Anreicherung im Tumor wird die breite Palette der gravierenden Nebenwirkungen reduziert. Aufgrund der Koppelung von MTX-HSA bleibt der Wirkstoff zudem wesentlich länger im gesamten Blutkreislauf des Körpers erhalten. Die pharmakologische Halbwertszeit von MTX-HSA liegt bei rund 19 Tagen. Das heißt, MTX-HSA entfaltet eine rund 150-fach längere Einwirkung gegenüber rein verabreichtem MTX – hier liegt die Halbwertszeit bei einer halben bis zu drei Stunden.
Wirkung bei unterschiedlichen, soliden Tumoren und Metastasen
Bereits in präklinischen Studien ab 1996 und mehreren klinischen Phase I/II-Studien zeigte das Albuminkonjugat MTX-HSA ein gutes Verträglichkeitsprofil und bei einigen der geprüften Tumorarten (insbesondere Nierenzellkarzinom und Pleuramesotheliom) auch eine tumorhemmende Wirkung, die man bei einer Therapie mit herkömmlichem Methotrexat nicht hätte erwarten können. Keine Auswirkungen konnte man bei Erkrankungen des blutbildenen Systems erkennen. 1 2 3 4
Aufgrund von Umstrukturierungen der beteiligten Pharmafirma wurde bis heute von der industriellen Zulassung von MTX-HSA abgesehen, so das Deutsche Krebsforschungsinstitut auf seiner Homepage.5
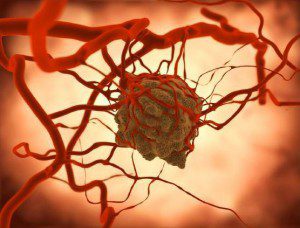
Solide Tumoren haben für das Wachstum einen erhöhten Energiebedarf, der unter anderem dadurch gedeckt wird, dass der Tumor große Mengen des Bluteiweißes Albumin über die Blutbahnen aufnimmt. ©Juan Gärtner – Fotolia
Da Albumin aus Geweben und Organen über die Lymphbahnen in den Kreislauf zurückgeführt wird und MTX-HSA sich wie ein natürliches Albumin verhält, können Lymphknotenmetastasen ebenfalls durch die systemische Verabreichung einer solchen kombinierten Verbindung erreicht werden.
Bei einer konventionellen Chemotherapie wird reines MTX in Kombination mit anderen Medikamenten bei verschiedenen Tumorerkrankungen eingesetzt, beispielsweise bei Mammakarzinomen oder zerebralen Lymphomen.
Entzündliche Prozesse / Rheumatoide Arthritis
Das Team vom DKFZ erkannte im Rahmen seiner Forschungen zudem, dass MTX-HSA auch bei entzündlichen Prozessen wie z.B. rheumatoider Arthritis erfolgreich eingesetzt werden kann.
Gesetzliche Grundlagen / Tumortherapie mit MTX-HSA
Bei MTX-HSA handelt es sich um die Koppelung von zwei bereits zugelassenen Stoffen (Methotrexat und Albumin). Das Konjugat kann über Apotheken mit den entsprechenden Voraussetzungen nach Arzneimittelgesetz hergestellt werden.
MTX-HSA als begleitende Therapie ermöglichen
In einer Phase-I-Studie im Jahr 2002 erschien eine zwei- bis dreiwöchige wöchentliche Applikation als gut verträglich.2 Die Behandlung von Patienten hat gezeigt, dass die Verabreichung von MTX-HSA oft zu einem krankheitsstabilisierenden Effekt führt, ohne die bekannten Nebenwirkungen einer Chemotherapie.
Intraoperative Tumordiagnostik
Parallel zur Koppelung von MTX an HSA entwickelte das Team am Deutschen Krebsforschungszentrum Heidelberg Ende der 80er-Jahre eine Methode zur Beladung von Albumin mit Fluoreszenzfarbstoff. Damit wurde die Möglichkeit für eine positive Tumordiagnostik geschaffen.
Ein albumingebundener Fluoreszenzfarbstoff, der in der intraoperativen Tumordiagnostik bei malignen Tumoren im Rahmen einer Phase I/II-Studie untersucht wurde, zeigte hohe Kontraste, geringes Ausbleichen und eine durch die Bindung an Albumin bedingte lange intrazelluläre Verweildauer im Tumor.1
Diese durch UV-Licht darstellbare Fluoreszenz stellt eine weitere Möglichkeit der intraoperativen Bildgebung und der Kontrolle während eines operativen Eingriffes dar. Die Tumorgängigkeit des Fluoreszenz-HSA-Konjugates ist der sichtbare Beweis für die Funktionsfähigkeit des Konzeptes der Nutzung von Albumin als Trägersubstanz.
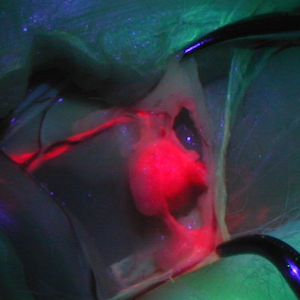
Die Darstellung von Lymphbahnen und Lymphknoten an der Fossa poplitea bei einem Kaninchen (rot) - 2 Stunden nach der Applikation von TCPC-Albumin unter D-Light. 6
Günstige Eigenschaften von Albuminkonjugaten
Entscheidend für das Verhalten der Konjugate sind die dominanten pharmakokinetischen Eigenschaften des Albumins. Durch die Bindung von Wirkstoffen an das Makromolekül Albumin erfolgt eine gezieltere Aufnahme in Tumoren. Dies beruht auf der günstigen Kinetik von Albumin mit einer Plasmahalbwertszeit von ca. 19 Tagen3, seiner hohen Kumulation in soliden Tumoren und der Bedeutung von Albumin als Tumornährstoff. Albumin als das dominierende Plasmaprotein ist die bedeutendste mobile Stickstoff- und Energiequelle für Tumoren und entzündliches Gewebe.
Die albumintypischen Eigenschaften bleiben nach der Koppelung erhalten. Damit wird eine rasche Elimination der Wirkstoffe durch das retikuloendotheliale System4 aus dem Kreislauf vermieden. Ebenso wie das Trägermolekül sind auch die Konjugate nicht immunogen. Das Konjugat kann sich durch die lange Präsenz im Blutkreislauf und aufgrund seiner makromolekularen Struktur in Tumoren anreichern.
Diese pharmakokinetischen Vorteile sind verantwortlich dafür, dass der alternative Aufnahmeweg des Konjugats in die Zelle wesentlich effizienter wird. Nach Endozytose bietet die lysosomale Freisetzung des Wirkstoffes innerhalb der Zelle die Möglichkeit, herkömmliche Resistenzmechanismen zu umgehen und gezielt Zellen mit potentiell hohem Eiweißbedarf anzugreifen.
¹ Eschen N, Bauder-Wüst U, Frei E, Schrenk HH, Sinn H, Kremer P, Kiprianova I, Hartung G.
Aminopterin-human serum albumin conjugate (AP-HSA): uptake and cytotoxic effects in tumor cell lines, In: Int. J.Clin .Pharmacol.Therapie, 2002
² Hartung G, Kremer P, Stehle G, et al., Phase I study of methotrexate-albumin in a bi-weekly intravenous bolus regimen in cancer patients, In: Proc. ASCO 19, 2000
³ Phase II study to assess the efficacy and tolerability of methotrexate-albumin (MTX-HSA) in the first line chemotherapy of patients with advanced malignant mesothelioma, 2002
4 Vis AN, van der Gaast A, van Rhijn BWG, Catsburg TK, Schmidt C, Mickisch GHJ. A phase II trial of methotrexate-human serum albumin (MTX-HSA) in patients with metastatic renal cell carcinoma who progressed under immunotherapy. Cancer Chemotherapy and Pharmacology 2002; 49:342-5.
5 DKFZ vom 28.Mai 2010: http://www.dkfz.de/de/praeventive-onkologie/pharmakologie.html, gespeichert am 25. Februar 2015
6 Kremer, P, Albumin als Carrier zur laserinduzierten Fluoreszenzdiagnostik und Chemotherapie maligner Tumoren. Habilitationsschrift an der Universitätsklinik Heidelberg, Abteilung für Neurochirurgie, 2002